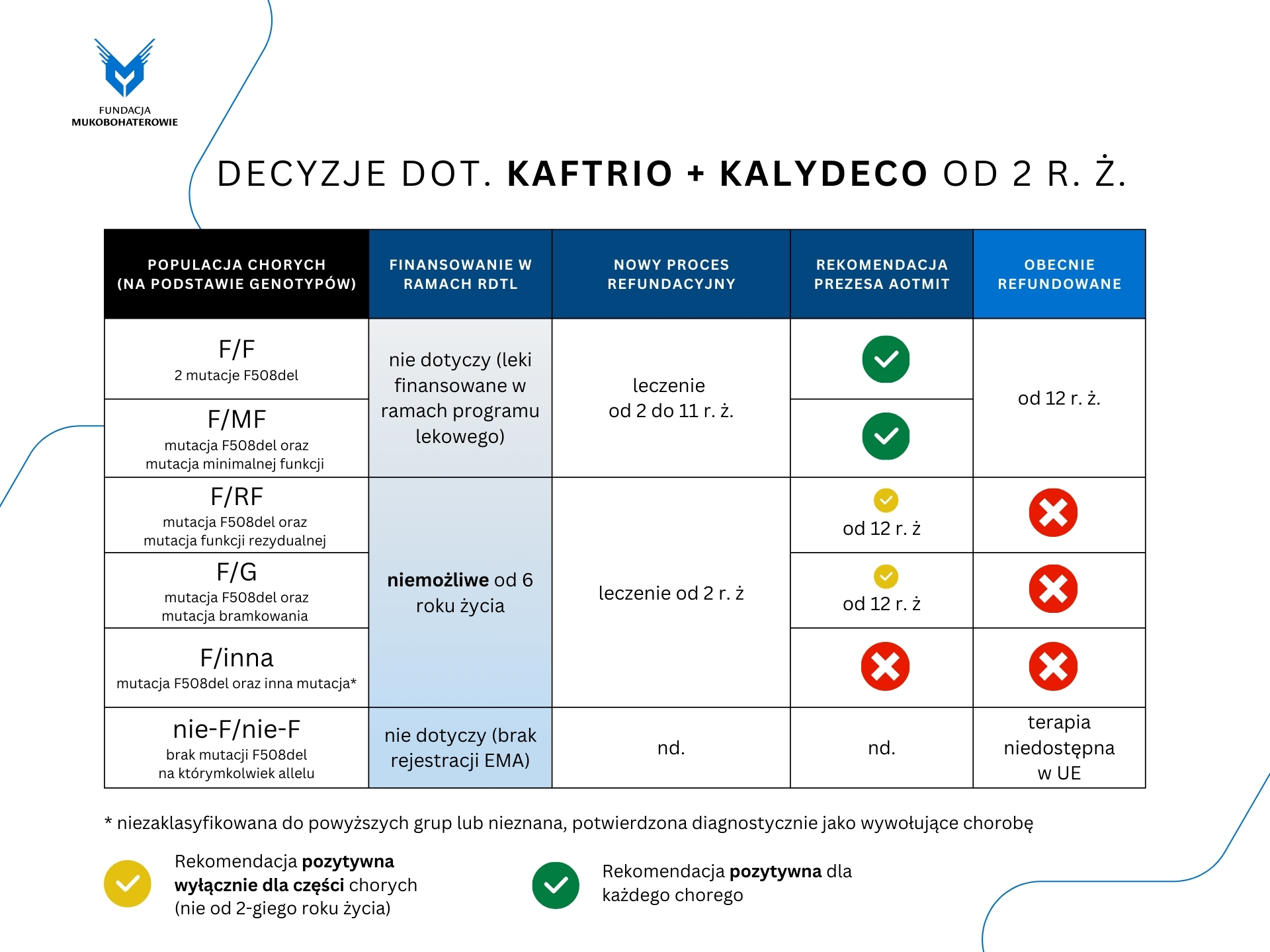
Do Wiceministra Zdrowia Marka Kosa zostało wystosowane pismo dotyczące zasadności usunięcia Kaftrio i Kalydeco z listy leków niepodlegających finansowaniu w ramach ratunkowego dostępu do technologii lekowych (RDTL). Przypominamy, że w listopadzie 2023 rok po raz pierwszy został wydany komunikat, który sprawił, że część chorych na mukowiscydozę nie może być leczona lekami sierocymi nawet w sytuacji konieczności ratowania ich życia lub zdrowia (patrz tabela poniej). Nie zmieniły tego kolejne komunikaty, w tym ostatni z 30 września 2024 roku. Sytuacja ta powinna ulec zmianie, gdyż 4 listopada 2024 roku, w ramach nowego postępowania refundacyjnego, Prezes Agencji Oceny Technologii Medycznych i Taryfikacji wydał pozytywną rekomendację dotyczącą zasadności objęcia refundacją produktów leczniczych.
W tej sprawie naszą fundację po raz kolejny wsparł adw. Marcin Pieklak oraz Magdalena Krupa-Polak z renomowanego zespółu prawników Life Sciences kancelarii prawnej Rymarz Zdort Maruta. W piśmie zostało przekazane, że:
(...) aktualna rekomendacja Prezesa Agencji w sprawie zasadności objęcia refundacją leków Kaftrio i Kalydeco:
- obejmuje szerszą populację pacjentów niż ta, o której była mowa w rekomendacji Prezesa Agencji nr 113/2022 z dnia 28 listopada 2022 r., oraz
- dotyczy także części pacjentów wykluczonych z dostępu do terapii finansowanej w ramach RDTL, tj. pacjentów w wieku co najmniej 6 lat i starszych, którzy posiadają co najmniej 1 mutację F508del w genie CFTR, a tym samym w jej skutek nie powinno dochodzić do dalszego ograniczania dostępu do terapii.
a tym samym w jej skutek nie powinno dochodzić do dalszego ograniczania dostępu do terapii.
(...) aby zapewnić spójność systemu ochrony zdrowia, transparentność działań instytucji publicznych oraz dostęp do bezpiecznej i skutecznej terapii dla chorych z mukowiscydozą komunikat Ministra Zdrowia w sprawie produktów leczniczych niepodlegających finansowaniu w ramach procedury RDTL, wydawany na podstawie art. 47f ust. 4 Ustawy o świadczeniach, powinien zostać zaktualizowany w zakresie możliwości finansowania leku Kaftrio i Kalydeco poprzez wykreślenie ww. leków z tego wykazu.
Poniżej przedstawiamy zaprezentowane przez nas stanowisko.

Kliknij na miniaturę, aby otworzyć w nowej karcie
Ratunkowy Dostęp do Technologii Lekowych to mechanizm finansowania szpitalom, ze środków publicznych, kosztów leków dla indywidualnego pacjenta w sytuacji, gdy wykorzystane zostały dostępne refundowane technologie lekowe i okazały się one nieskuteczne dla ratowania jego życia lub zdrowia.
Obecnie znanych jest ponad 2000 mutacji genu oznaczonego jako CFTR, z czego około 1000 skutkujących wystąpieniem mukowiscydozy. Mukowiscydoza jest ciężką chorobą wielonarządową, spowodowaną wadą obu alleli CFTR. Spora liczba mutacji choroby powoduje dużą różnorodność w populacji pacjentów, w konsekwencji utrudnia badania kliniczne i dzieli pacjentów na podgrupy i dedykowane im leczenie.
Leki Kaftrio i Kalydeco (kosztujące pacjenta komercyjnie nawet 80 tys. złotych miesięcznie) są refundowane w Polsce od marca 2022 roku dla grupy docelowej około 1 tys. z 2 tys. chorych na mukowiscydozę. W Polsce terapia jest dostępna dla chorych powyżej 12 roku życia z konkretnymi mutacjami choroby.
Według aktualnie obowiązującego programu lekowego, finansowanie ze środków publicznych jest dostępne dla chorych spełniających łącznie dwie przesłanki (poza kryterium wieku i szeregiem innych wytycznych dotyczących stanu zdrowia): posiadających przynajmniej jedną mutację F508del (najczęściej występująca) i drugą mutację selektywnie określoną tzw. minimalnej wartości funkcji (zgodnie z wcześniej prowadzonymi badaniami klinicznymi). Po pewnym czasie skuteczność i bezpieczeństwo leków stwierdzono dla chorych powyżej 2 roku życia (nie jak dotychczas 12 lat – a zatem chorych znacznie młodszych) i dla większej liczby mutacji mukowiscydozy (wystarczy, aby chory miał przynajmniej jedną mutację F508del, a to dotyczy ok. 85% chorych w Polsce). Przyznały to agencje dopuszczające leki na rynek amerykański (FDA) i europejski (EMA). Wprowadzenie leczenia dla nowych grup pacjentów wymaga rozpatrzenia nowego wniosku refundacyjnego, a ten został złożony przez firmę Vertex Pharmaceuticals 23 kwietnia 2024 roku. To już drugie postępowanie administracyjne dotyczące rozszerzenia dostępu do leków. Poprzednie zostało umorzone po złożeniu wniosku przez firmę farmaceutyczną.