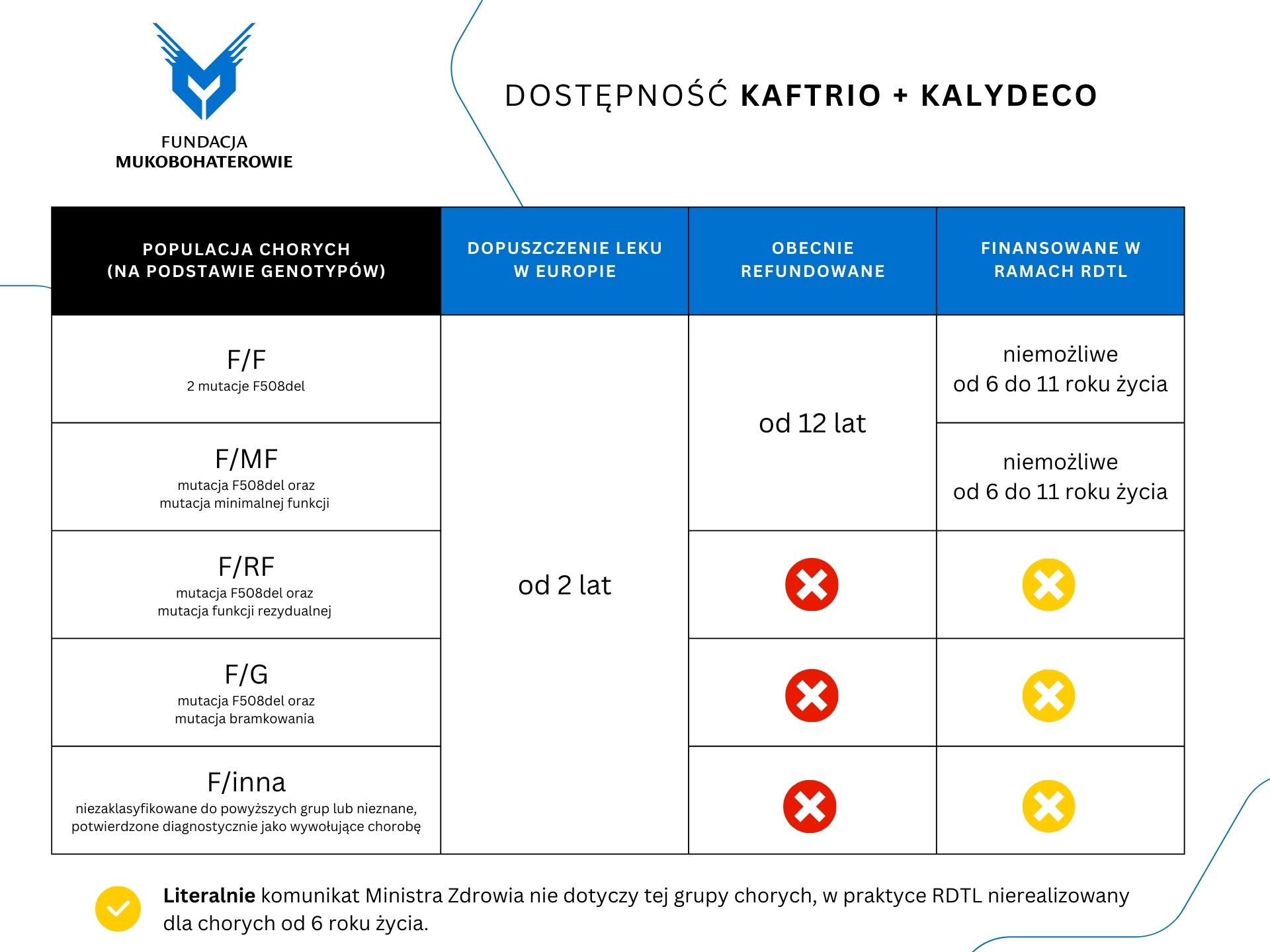
Do Wiceministra Zdrowia Macieja Miłkowskiego zostało wystosowane pismo dotyczące zasadności usunięcia z listy leków niepodlegających finansowaniu w ramach ratunkowego dostępu do technologii lekowych (RDTL). Przypominamy, że w listopadzie 2023 roku został wydany komunikat, w którego sprawie pisaliśmy do Rzecznika Praw Obywatelskich. Sprawił on, że część chorych na mukowiscydozę nie może być leczona lekami sierocymi nawet w sytuacji konieczności ratowania ich życia lub zdrowia (patrz tabela poniej).
W odpowiedzi na wystąpienie Rzecznika Praw Obywatelskich Marcin Wiącka przedstawiciel resortu zdrowia jako podstawę prawną dla podjętego działania podał art. 47f ust. 3 ustawy z dnia 27 sierpnia 2004 r. o świadczeniach opieki zdrowotnej finansowanychze środków publicznych. Z przedstawionej argumentacji wynika, że chodziło o pkt 3 przepisu. Nie zgadzamy się z tym stanowiskiem. W tej sprawie naszą fundację po raz kolejny wsparł adw. Marcin Pieklak oraz Magdalena Krupa-Polak z renomowanego zespółu prawników Life Sciences kancelarii prawnej Rymarz Zdort Maruta. W piśmie zostało przekazane, że:
(...) na podstawie aktualnie obowiązującego obwieszczenia refundacyjnego pacjenci chorujący na mukowiscydozę:
- w wieku od 6 do 11 lat, którzy mają co najmniej jedną mutację F508del genu CFTR oraz
- w wieku od 12 lat, którzy mają co najwyżej jedną mutację F508del genu CFTR oraz dodatkowo drugą mutację inną niż określana jako minimalna wartość funkcji (MF)
nie mają dostępu do bezpłatnej terapii eleksakaftorem/ tezakaftorem /iwakaftorem w skojarzeniu z iwakaftorem.
A zatem okazuje się, że pacjenci chorujący na mukowiscydozę z niektórymi mutacjami, w szczególności pacjenci powyżej 12 roku życia (przy czym należy mieć na uwadze, że choroba postępuje wraz ze starzeniem się chorego) oraz młodsi chorzy w obecnej chwili nie mogą korzystać z szansy ratowania życia lub zdrowia przy pomocy modulatorów CFTR.
Pragnę jednocześnie dodać, że mukowiscydoza jest chorobą, która wywołuje w organizmie pacjenta nieodwracalne zmiany, co rzutuje oczywiście w istotnym stopniu na nastoletni oraz dorosły okres życia młodego pacjenta
(...) w Rekomendacji Prezes Agencji zarekomendował objęcie refundacją leków Kaftrio i Kalydeco we wskazaniu: pacjenci w wieku co najmniej 6 lat homozygotyczni pod względem mutacji F508del genu CFTR lub heterozygotyczni pod względem mutacji F508del z mutacją o minimalnej wartości funkcji (MF) genu CFTR pod warunkiem pogłębienia instrumentu dzielenia ryzyka oraz zaproponowania dodatkowego instrumentu dzielenia ryzyka zabezpieczającego całkowity wpływ na budżet płatnika.
Prezes Agencji nie wydał zatem do tej pory rekomendacji o niezasadności objęcia ww. leków refundacją. Wydanie przez Prezesa Agencji rekomendacji warunkowej nie może być bowiem utożsamiane z wydaniem rekomendacji negatywnej. Przeczy temu przede wszystkim jej literalne brzmienie. Uznanie, iż niespełnienie przez podmiot odpowiedzialny warunku, o którym mowa w rekomendacji Prezesa Agencji niejako „zmienia” charakter rekomendacji z „pozytywnej warunkowej” na negatywny jest całkowicie nieuzasadnione i nie znajduje oparcia w powszechnie obowiązujących przepisach prawa.
Co więcej, przesłanki, o których mowa w art. 47f ust. 3 Ustawy o świadczeniach nie mogą być odczytywane w sposób rozszerzający zakres sytuacji która ogranicza możliwość zastosowania mechanizmu RDTL. Celem RDTL jest bowiem zapewnienie pacjentom ostatniej szansy na skuteczną terapię pozwalającą na uratowanie ich życia lub zdrowia w momencie, w którym inne terapie zawiodły.
Należy jednoznacznie podkreślić, że stosowanie przedstawionej powyżej interpretacji art. 47f ust. 3 pkt 3 Ustawy o świadczeniach, tzn. interpretacji wskazującej na to, że „rekomendacją w zakresie niezasadności objęcia refundacją leku” jest także rekomendacja pozytywna warunkowa, powodowałoby nieuzasadnione ograniczenie dostępu pacjentów do terapii ratujących ich życie lub zdrowie.
Poniżej przedstawiamy wystąpienie Rzecznika Praw Obywatelskich, odpowiedź Wiceministra zdrowia oraz zaprezentowane przez nas stanowisko.



Kliknij na miniaturę, aby otworzyć w nowej karcie
Ratunkowy Dostęp do Technologii Lekowych to mechanizm finansowania szpitalom, ze środków publicznych, kosztów leków dla indywidualnego pacjenta w sytuacji, gdy wykorzystane zostały dostępne refundowane technologie lekowe i okazały się one nieskuteczne dla ratowania jego życia lub zdrowia.
Obecnie znanych jest ponad 2000 mutacji genu oznaczonego jako CFTR, z czego około 700 skutkujących wystąpieniem mukowiscydozy. Mukowiscydoza jest ciężką chorobą wielonarządową, spowodowaną wadą obu alleli CFTR. Spora liczba mutacji choroby powoduje dużą różnorodność w populacji pacjentów, w konsekwencji utrudnia badania kliniczne i dzieli pacjentów na podgrupy i dedykowane im leczenie.
Leki Kaftrio i Kalydeco (kosztujące pacjenta komercyjnie nawet 80 tys. złotych miesięcznie) są refundowane w Polsce od marca 2022 roku dla grupy docelowej około 1 tys. z 2 tys. chorych na mukowiscydozę. W Polsce terapia jest dostępna dla chorych powyżej 12 roku życia z konkretnymi mutacjami choroby.
Według aktualnie obowiązującego programu lekowego, finansowanie ze środków publicznych jest dostępne dla chorych spełniających łącznie dwie przesłanki (poza kryterium wieku i szeregiem innych wytycznych dotyczących stanu zdrowia): posiadających przynajmniej jedną mutację F508del (najczęściej występująca) i drugą mutację selektywnie określoną tzw. minimalnej wartości funkcji (zgodnie z wcześniej prowadzonymi badaniami klinicznymi). Po pewnym czasie skuteczność i bezpieczeństwo leków stwierdzono dla chorych powyżej 6 roku życia (nie jak dotychczas 12 lat – a zatem chorych znacznie młodszych) i dla większej liczby mutacji mukowiscydozy (wystarczy, aby chory miał przynajmniej jedną mutację F508del, a to dotyczy ok. 81% chorych w Europie). Przyznały to agencje dopuszczające leki na rynek amerykański (FDA) i europejski (EMA). Wprowadzenie leczenia dla nowych grup pacjentów wymaga rozpatrzenia nowego wniosku refundacyjnego. Ten został złożony przez firmę Vertex Pharmaceuticals (Poland) Sp. z o.o. 31 maja 2022 roku, ale po długotrwałych negocjacjach podmiot wycofał go. Podczas trwania procesu administracyjnego Prezes Agencji Oceny Technologii Medycznych i Taryfikacji (dalej Prezes AOTMiT) wydał Rekomendację nr 113/2022 z 28 listopada 2022 r. Rekomendacja stanowiła, że „Prezes Agencji rekomenduje objęcie refundacją produktów leczniczych (…) pod warunkiem pogłębienia instrumentu dzielenia ryzyka oraz zaproponowania dodatkowego instrumentu dzielenia ryzyka zabezpieczającego całkowity wpływ na budżet płatnika.”.